Environment Modulates Protein Heterogeneity Through Transcriptional and Translational Stop Codon Miscoding
Stop codon miscoding events give rise to longer proteins, which may alter the protein’s function and thereby generate short-lasting phenotypic variability from a single gene. In order to systematically assess the frequency and origin of stop codon miscod
www.biorxiv.org
Toth-Petroczy Group
2023, bioRxiv
Abstract
종결코돈 miscoding 은 긴 단백질을 만들고, 이는 단백질의 기능을 바꿔 짧게 지속되는 표현형적 다양성을 야기할 수 있다. (역주 : miscoding 이므로 genetic mutation 이 아니고, 영구적이지 않은 짧은 표현형을 야기할 수 있다는 뜻 )
종결코돈 miscoding 의 빈도와 origin 을 종합적으로 평가하기 위해서, 우리는 reporter library 를 디자인했다. 우리는 premature 종결 코돈을 mScarlet 에 도입하여, E.coli 에서 형광현미경을 이용해 단백질 합성 종결 오류의 high-throughput 정량화를 가능하게 했다.
우리는 스트레스 조건에서 뉴클레오티드 맥락에 따라 80%까지 높은 비율로 종결코든 miscoding 이 발생할 수 있다는 것을 발견했으며, 진화가 종종 종결코든 miscoding event 를 sample 한다는 것을 의미한다.
MS와 RNA-seq 을 통한 선택된 reporter 들의 분석은 종결코든 miscoding 에 번역 오류 뿐만 아니라 전사 오류도 기여한다는 것을 보여준다. RNA 중합효소는 premature 종결코돈에 뉴클레오타이드를 잘못 도입하는 경향이 있다.
MS 를 통한 종결코돈 miscoding 의 단백질체 수준의 검출은 온도가 E.coli 에서 종결코돈 miscoding 으로 인해 생성된 암호화된 서열의 발현을 조절한다고 밝혔다.
전체적으로, 우리의 연구결과는 환경이 단백질 생산의 정확성에 영향을 주며, 이는 개체들이 새로운 환경에 적응이 필요할 때 단백질 heterogeneity 를 증가시킨다고 제시한다.
Introduction
단백질 합성 종결은 높은 정확도를 가지게 최적화되지만 완벽하지 않음. 지구에 있는 모든 생명체들에서 번역 종결은 종결토돈에 의해 이루어지고 방출인자에 의해서 촉매됨. 이 과정은 canonical-size 의 단백질에 유전적 정보를 다시 쓰게 진화됨. 하지만 종결코돈 miscoding (SCM) 은 종결 코돈에 RNA 중합효소가 뉴클레오타이드를 잘못 도입하는 전사 오류나 리보솜이 tRNA 를 잘못 도입하는 경우인 번역 오류로 인해서 일어날 수 있음. 이러한 오류들은 C-termini 가 연장된 단백질 변이를 만들어내게 되고, 한 유전자로부터 다양한 길이를 가지는 단백질의 population 을 만들어내게 됨.
종결코돈 miscoding 에서 오는 단백체의 다양화는 표현형적 다양성을 야기할 수 있고, 이는 세포의 운명을 결정함. 예를 들어 단백질 합성 종결의 비정확성은 적응적이고 기능적일수도 있지만, 비적응적일수도 있어서 어떤 때는 적응도(Fitness) 의 감소를 가져오기도 함. 또한, 리보솜을 미끄러지게 하여 코돈 읽기를 정지시키는 정지 코돈 업스트림의 "Slippery Sequence" 는 종종 기능함. 전사, 번역 오류는 유전체 변이보다 짧게 지속되는 표현형적 다양성을 만들 수 있음. 따라서 SCM 은 갑작스러운 환경의 변화에 따른 빠른 적응을 가능하게 함. 이러한 엄청난 진화적인 암시는 살아있는 상태에서 단백질 합성 종결의 비정확성을 설명할 수 있는 규칙에 대한 연구에 대한 필요성을 보임.
몇몇 연구들은 다양한 환경조건 아래에서 종결코돈 miscoding 의 연관성을 강조하고 있음. carbon starvation 과 과도한 glucose 는 pH 를 낮추며 E.coli 에서 TGA 의 readthrough 를 야기함. 그러나 이러한 연구는 주어진 정지 코돈과 유전적 맥락에 대한 정보를 제공하여 락토스로 보충된 LB에서 세포가 성장했을 때 최대 14%의 TGA 판독을 검출함. 더 나아가, 낮은 성장 온도는 Bacillus subtilis 에서 ribosomal frameshift 를 급격하게 증가시킴. 반면에 SCM의 온도에 대한 impact 는 알려진바가 없음.
이 연구에서는 다양한 유전적인 context 와 다른 온도, 영양 조건 하에서 모든 종결코돈에 대한 단백질 합성 종결의 비정확성을 종합적으로 확인하였음.
주된 질문들은 이것들이었음 :
1) 단백질 합성 종결 시 어느 정도 빈도로 오류가 발생하는가?
2) 비위험 환경 조건이 진화가 이러한 사건을 만날 기회를 조절하는지 여부
3) 그들이 어디서부터 온 것인지? 전사과정 중인지, 번역과정 중 인지.
우리는 형광현미경을 이용해 E.coli 에서 단백질 합성 종결의 오류를 정량화하게 한 리포터를 디자인했음. 우리는 mScarlet 서열에서 43개의 모호한 위치를 target 했으며, 야생형의 코돈을 3개 종결코돈 중 하나로 돌연변이시켰음. 따라서 단백질 합성 종료를 건너뛰는 오류가 발생할 경우에만 전체 길이 mScarlet이 합성됨.
우리는 단백질 종결 정확도가 stop codon 의 유전적 맥락과 identity 에 의지한다고 확인했음. 따라서 우리는 단백질 서열에서 단백질 합성 종결 오류에 취약한 hotspot 들을 예측하는 규칙들을 만들었음. 우리는 또한 낮은 온도나 영양부족같은 환경적 스트레스 조건 하에서 stop codon 의 miscoding 확률이 증가됨을 보였음.
그에 따라, E.coli의 proteome 28% 를 차지하고 있는 opal stop codon 인 TGA 는 특정 스트레스 조건과 특정 given nucleotide context 하에서 최대 80% 의 비율로 단백질 합성 종결에 실해했음. 선택된 reporter 들에서의 RNA-seq 과 MS 결과는 단백질 합성 종결의 오류가 리보좀 readthrough 로부터만 온 것이 아니라, RNA 중합효소 오류도 기여한다는 사실을 보임. 우리는 RNA 중합효소가 좀 더 premature stop codon 에 뉴클레오타이드를 잘못 도입한다는 사실을 밝힘.
마지막으로, E.coli 의 proteome 분석은 SCM 으로부터 밝혀진 암호화된 서열의 존재와, SCM 을 좀 더 자연적인 문맥 상에서 예측하기 위한 우리의 rule 을 확인시켜주었음.
전반적으로, 우리의 연구 결과는 환경과 영구적인 생물학적 흐름 사이의 crosstalk을 시사한다.
Result
Visualizing and quantifying stop codon readthrough events in E. coli
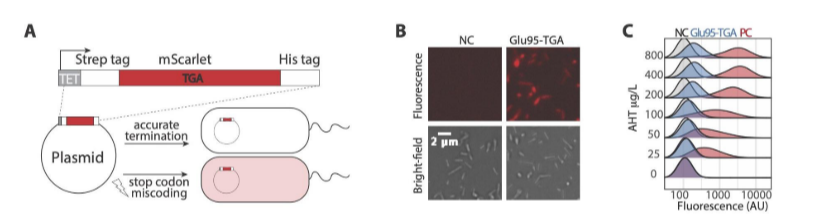
SCM 이 시각화, 정량화될 수 있는 fluorescence reporter 제작
- mScarlet allele 에 premature stop codon 을 끼워넣는 방식. Strep Tag, His Tag 는 protein 정량화시에 사용됨
- 정상적으로 번역이 일어나면 full-length mScarlet 이 합성 안되고, 오류가 일어났을시에만 mScarlet 이 합성됨.
- 먼저 mScarlet 의 95번 자리에 TGA 종결코돈 도입했음.
- Reporter 의 발현을 정밀하게 조절하기 위해, low copy number vector 와 inducible promoter을 사용했다고 함.
- 실험을 위해 WT E.coli에 Gly95-TGA reporter를 도입.
- Low copy number vector : reporter gene의 copy 를 소량 가지고 있는 플라스미드로, 숙주세포에서 과발현과 독성을 줄이는 목적임.
- Inducible promoter : 배지에 특정 화합물을 첨가함으로서 on/off 가 가능한 promoter sequence. 유전자 발현의 정확한 조절을 가능하게함
NC : Negative Control ; PC : Positive control with WT mScarlet
- Inducer 의 농도가 높을수록 TGA, PC 에서의 신호가 센 것을 볼 수 있음.
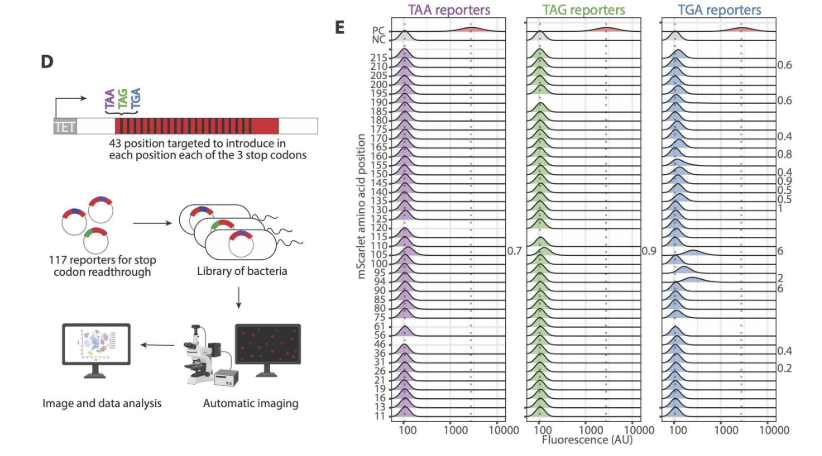
37℃ in rich media 에서 키운 E. coli 세포들.
- SCM 의 "propensity" 는 PC 와 비교해서 median fluorescence 가 몇 % 정도인가로 계산됨. 확인할 수 있는 것은 랜덤하게 고른 mScarlet 의 43 개 자리 중에서 유독 SCM event 가 잘 일어나는 hotspot 이 존재한다는 것.
- 또한 SCM 이 잘 일어나는 종결코돈의 트렌드도 존재 : TGA > TAG > TAA
- SCM event 가 꽤 자주 일어난다는 것을 볼 수 있었는데, 이는 PC 의 fluorescence median 과 비교해서 몇 % 정도인가로 계산. Gly95-TGA reporter 의 2.1% 정도에서 단백질 합성이 실패한다는 것을 볼 수 있었음.
Non-optimal growth temperatures and nutrient scarcity promote stop codon miscoding.
 |
 |
- Rich media 에서 자란 경우를 확인해보면 온도에 따라서 SCM level 이 상당히 다름. 18℃ 에서 SCM event 가 잦음. 또한 TAA 가 제일 정확하게 단백질 합성을 종결 ( 온도가 낮아도 SCM 없이 정상적으로 번역이 진행됨 ). TGA 가 SCM 이 제일 잦음.
- Minimum 배지에서 키웠을 때 온도가 낮아지면 SCM 증가, TAA 가 제일 정확, TGA 가 제일 정확하지 않음( 위의 결과와 동일)
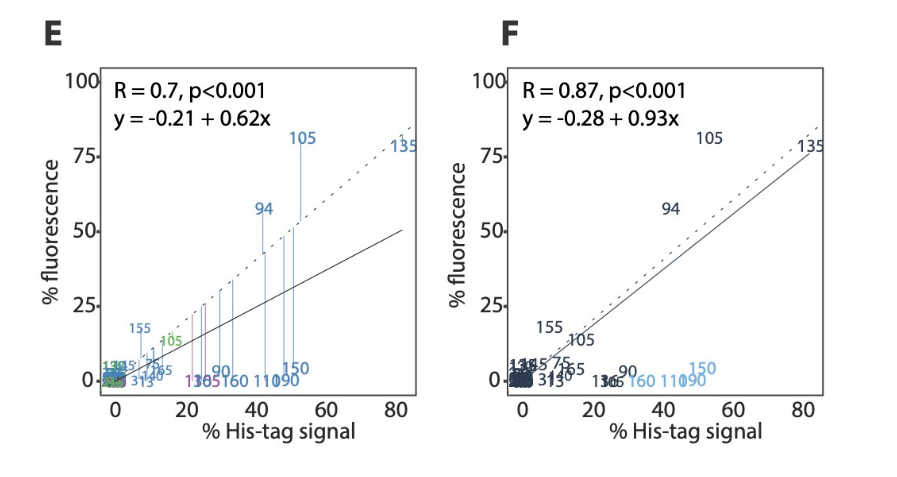
- 연구에서 mScarlet 의 형광 신호와 SCM 을 묶어서 생각했지만, SCM 이 mScarlet 의 4차 구조나 2차 구조에 영향을 줘서, Full-length 이긴 하지만 작동하지 않는 경우나, 과다 형광을 내는 경우도 있을 것이라 생각했음.
- 따라서 우리가 제작한 fluorescence reporter library 의 한계점을 평가하고 SCM 을 검출하는 orthologous 한 방법을 사용했음. 리포터는 His tag 을 가지고 있는데, 따라서 SCM 의 경우에만 His-tag 가 생성됨. Western blot 을 사용하여 SCM 을 검출하는 방법을 고안했음.
- 결과 상에서 his-tag signal ( SCM 의 결과로 생기는 signal ) 과 Fluorescence signal ( SCM 의 결과로 생기지만 bias 가 존재할 수 있는 siganl ) 의 correlation 은 상당했지만 이른바 "Dark reporter" 가 존재했음 ( His-tag signal 은 있지만 Fluorescence signal 은 없는)
- "Dark reporter" 를 제거한 결과 상관관계가 더 좋아졌음. 구조에 대한 관계는 추가 실험이 필요함.
High G and low T content downstream of the stop codon increases the likelihood of stop coding miscoding
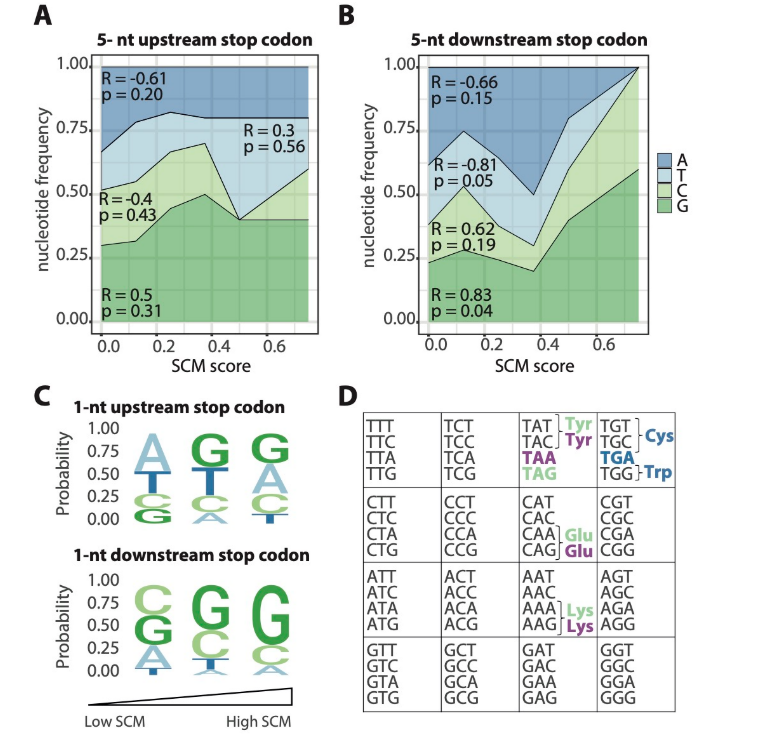
- SCM 이 주어진 위치에서 얼마나 있을지에 대한 score 를 계산함 ( 각 position 별로 계산됨 ). 그 후 5-nt up, downstream 으로 염기의 context 비율에 따라서 그 score 를 확인함.
- Positive correlation for G and negative for T content downstream of the premature stop codon
- Downstream region after the premature stop codon influences the SCM rate. While G increases the SCM propensity, T has the opposite effect.
Low RNA polymerase accuracy at premature stop codons.
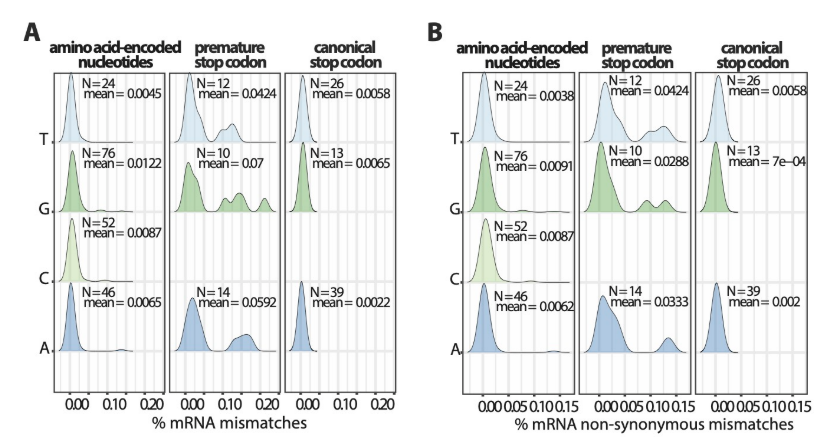
- Premature stop codon 에서의 RNA 중합효소 mismatching 의 확률이 더 큼. 또한, RNA polymerase 의 주변 서열은 RNA 중합효소의 정확성에 영향을 미치지 않음.
Proteome-wide mass spectrometry detects stop codon miscoding events in 32 peptides mapping to 28 proteins in E. coli.
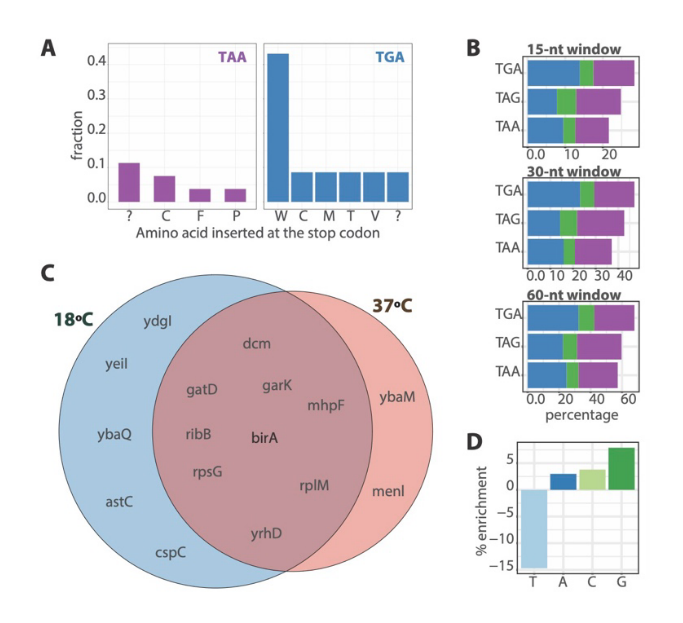
0.45% of TAA E. coli proteins ; 1.35% of TGA E. coli proteins.
B) The occurrence of an additional stop codon in a 15, 20, and 30-nt window downstream of the stop codon correlates with the protein synthesis accuracy of the stop codon in E. coli genome.TAG, as the least accurate stop codon, has the highest frequency of an additional stop codon in the 3’ regions of genes.
C) 9개의 유전자가 18도 조건 하에서만 유일하게 관찰되는 것을 볼 수 있었음. 이는 Cryptic sequence 로 말할 수 있고, 짧게 말해 일반적인 상태에서는 발현되거나 번역되지 않다가 특정 조건 하에서만 나오는 서열임. 이는 이전에 알려져있지 않은 유전적 다양성이나 표현형적 유연성을 나타낼 수 있음.
The cryptic sequences are protein-coding sequences that are normally not expressed or translated in E. coli cells under normal growth conditions but can be activated or "unlocked" by specific environmental stimuli, such as cold shock. The authors hypothesized that bacteria could use errors in protein synthesis termination, such as stop codon readthrough, as a mechanism to rapidly diversify their proteome and adapt to sudden changes in their surroundings. To test this hypothesis, they detected cryptic sequences among the E. coli proteome that were only expressed by stop codon readthrough under cold shock conditions . These cryptic sequences may represent a previously unrecognized source of genetic diversity and phenotypic plasticity in bacteria and could have important implications for understanding bacterial adaptation and evolution.
D) Downstream 에 G 가 있으면 단백질 합성 종결 정확도를 감소시키지만, T 는 증가시킨다 ( SCM 의 enrichment 임 ).
Discussion
- 이 논문은 대장균에서 종결코돈 미스코딩 (SCM) 이벤트가 빈번하게 발생하며, 이러한 이벤트의 발생률은 종결코돈의 신원, 유전자 맥락, 성장 온도 또는 영양소와 같은 내부 요인과 외부 요인에 의해 변화된다는 것을 보여준다는 내용
- 또한, 종결코돈의 정확도에 대한 불확실성이 단백질 합성 종결 오류의 광범위한 돌연변이 공간을 도입한다는 것을 분석
- 이 연구 결과를 토대로 대장균에서 단백질 발현 벡터를 설계할 때 TGA를 피하고, 종결코돈 이후 하류 영역을 최적화하는 것을 제안
- 또한, 이 논문은 단백질 합성 종결 오류가 세포의 환경 변화에 빠르게 적응하기 위한 기전으로 작용할 수 있다는 가설을 제시
- 최종적으로, 이 연구 결과는 단백질 다양성을 증가시키는 데에 있어서 전사 및 번역 오류가 중요하게 작용한다는 것을 보임
'논문 리뷰 > Protein' 카테고리의 다른 글
| Global detection of human variants and isoforms by deep proteome sequencing (0) | 2023.05.11 |
|---|---|
| [Archive] Intrinsically Disordered Proteins ( IDPs ) (0) | 2023.04.10 |
| [Archive] Condensates and phase separation (0) | 2023.04.10 |
| AlphaFold and Implications for Intrinsically Disordered Proteins (0) | 2023.04.10 |
| Liquid–liquid phase separation in tumor biology (0) | 2023.04.10 |


댓글